
Fil d'Ariane
- Nouvelles et événements
- Nouvelles
- Content
- Un consortium international étudie les cellules immunitaires hyperactives comme cause possible des décès dus à la COVID-19
null Un consortium international étudie les cellules immunitaires hyperactives comme cause possible des décès dus à la COVID-19
Une nouvelle publication établit un lien entre l'infiltration de neutrophiles dans les poumons des patients et les symptômes de la COVID-19
16 avril 2020
Montréal – Dans la bataille urgente pour traiter les patients atteints de COVID-19, un groupe de onze organisations internationales de recherche médicale étudie si les cellules immunitaires hyperactives qui produisent des pièges extracellulaires de neutrophiles (dits Neutrophil Extracellular Traps ou NETs) sont à l'origine des cas les plus graves. Le consortium, appelé NETwork, comprend le Laboratoire Cold Spring Harbor, les Feinstein Institutes for Medical Research et l'Institut de recherche du Centre universitaire de santé McGill (IR-CUSM).
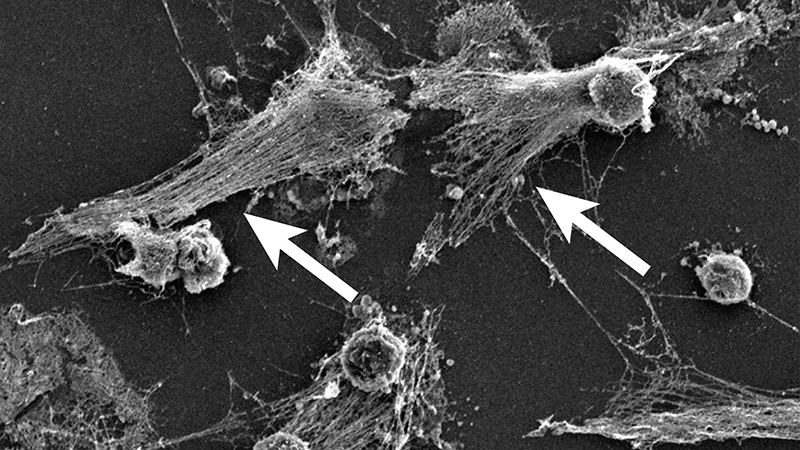
Un article publié aujourd'hui dans le Journal of Experimental Medicine décrit que les patients atteints d'une infection grave causée par la COVID-19 développent un syndrome de détresse respiratoire aiguë (SDRA), une inflammation pulmonaire, d’épaisses sécrétions de mucus dans les voies respiratoires, des lésions pulmonaires étendues et des caillots sanguins. Ce stade avancé de la maladie est difficile à gérer. Dans le pire des cas, les patients ont besoin d'une ventilation mécanique invasive, et néanmoins, un grand nombre de patients meurent. L’équipe de NETwork suggère que la gravité de la COVID-19 pourrait résulter de l'hyperactivité des globules blancs appelés neutrophiles. Les neutrophiles, qui font partie du système immunitaire de l'organisme, détectent les bactéries et peuvent expulser leur ADN pour les attaquer à l'aide d'un réseau d'ADN attaché à des enzymes toxiques, appelé NET. Ces NETs peuvent piéger et digérer l'agent pathogène indésirable, mais dans les cas de SDRA, ils endommagent les poumons et d'autres organes.
« Étant donné les similitudes évidentes entre la présentation clinique de la COVID-19 grave et d'autres maladies connues provoquées par les NETs, telles que le SDRA, nous proposons que l'excès de NETs puisse jouer un rôle majeur dans la maladie », a déclaré Betsy Barnes, PhD, auteure principale et co-correspondante de l'article et professeure aux Feinstein Institutes. « Au fur et à mesure que des échantillons de patients seront disponibles, il sera important de déterminer si la présence de NETs est associée à la gravité de la maladie et/ou à des caractéristiques cliniques particulières de la COVID-19 ».
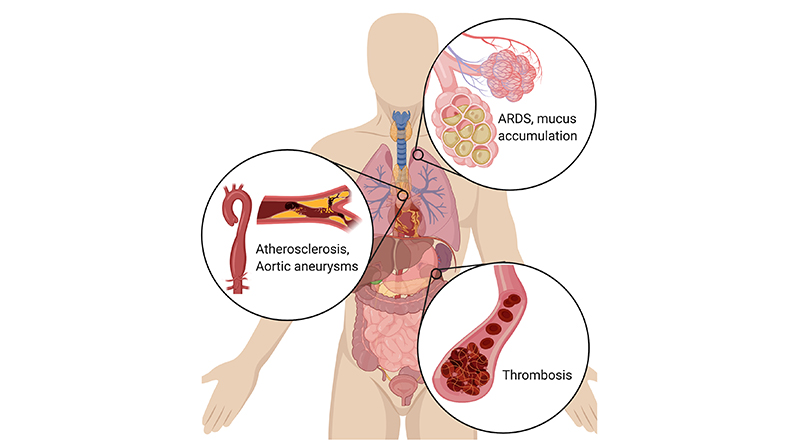
« Les NETs ont été identifiés en 2004, mais de nombreux scientifiques n'en ont jamais entendu parler. La plupart des chercheurs du groupe NETwork ont travaillé sur des NETs présents dans d'autres maladies, et quand nous avons commencé à entendre parler des symptômes des patients atteints de COVID-19, cela nous a semblé familier, » a déclaré Mikala Egeblad, biologiste du cancer au Laboratoire Cold Spring Harbor, auteure co- correspondante de l'article qui a réuni le groupe de recherche du NETwork autour de la COVID-19.

Jonathan Spicer, MD PhD, clinicien-chercheur à l'IR-CUSM et professeur adjoint de chirurgie à l'Université McGill, est un chirurgien thoracique qui a été témoin des effets dévastateurs de la COVID-19 au chevet des patients. « Nous voyons chez ces patients des lésions pulmonaires graves connues sous le nom de SDRA, un autre problème sérieux causé par un excès de NETs et observé dans les cas sévères de grippe, a-t-il déclaré. Leurs voies respiratoires sont souvent obstruées par un mucus épais et, contrairement à ce que l’on observe pour la plupart des infections pulmonaires graves, ces patients ont tendance à former de petits caillots dans tout leur corps à un rythme beaucoup plus élevé que la normale. Des NETs ont également été trouvés dans le sang de patients atteints de septicémie ou de cancer, où ils peuvent faciliter la formation de tels caillots ».
Les chercheurs des onze institutions membres du groupe NETwork poursuivent actuellement des études pour savoir si les NETs sont une caractéristique commune des cas de COVID-19. Si leurs conclusions montrent que les excès de NETs provoquent les symptômes graves de la COVID-19, alors une nouvelle piste thérapeutique pourrait être envisagée pour aider les patients atteints de COVID-19. Les traitements actuels utilisés pour d'autres maladies causées par les NETs ou les neutrophiles –comme la fibrose kystique, la goutte et la polyarthrite rhumatoïde– pourraient atténuer l'activité des NETs chez les patients atteints de COVID-19, réduisant ainsi le besoin de recourir à une ventilation mécanique invasive.
Les instituts de recherche suivants font partie du groupe NETwork: le Laboratoire de Cold Spring Harbor, les Feinstein Institutes for Medical Research, l'Institut de recherche du Centre universitaire de santé McGill., le Weill Cornell Medicine, la Donald and Barbara Zucker School of Medicine at Hofstra/Northwell, le Centre hospitalier universitaire de Nancy, l’Université du Michigan, l’Université de Californie à San Francisco, l’Université du Texas, le MD Anderson Cancer Center, l’École de médecine de l’Université de l’Utah et Northwell Health.
About Cold Spring Harbor Laboratory
Founded in 1890, Cold Spring Harbor Laboratory has shaped contemporary biomedical research and education with programs in cancer, neuroscience, plant biology and quantitative biology. Home to eight Nobel Prize winners, the private, not-for-profit Laboratory is a National Cancer Institute designated Cancer Center, employing 1,100 people including 600 scientists, students and technicians. The Meetings & Courses Program annually hosts more than 12,000 scientists. The Laboratory’s education arm also includes an academic publishing house, a graduate school and the DNA Learning Center with programs for middle and high school students and teachers. For more information, visit www.cshl.edu
About the Feinstein Institutes
The Feinstein Institutes for Medical Research is the research arm of Northwell Health, the largest health care provider and private employer in New York State. Home to 50 research labs, 2,500 clinical research studies and 5,000 researchers and staff, the Feinstein Institutes raises the standard of medical innovation through its five institutes of behavioral science, bioelectronic medicine, cancer, health innovations and outcomes, and molecular medicine. We make breakthroughs in genetics, oncology, brain research, mental health, autoimmunity, and are the global scientific leader in bioelectronic medicine – a new field of science that has the potential to revolutionize medicine. For more information about how we produce knowledge to cure disease, visit feinstein.northwell.edu.
About the Research Institute of the McGill University Health Centre
The Research Institute of the McGill University Health Centre (RI-MUHC) is a world-renowned biomedical and healthcare research centre. The Institute, which is affiliated with the Faculty of Medicine of McGill University, is the research arm of the McGill University Health Centre (MUHC) – an academic health centre located in Montreal, Canada, that has a mandate to focus on complex care within its community. The RI-MUHC supports over 460 researchers and close to 1,300 research trainees devoted to a broad spectrum of fundamental, clinical and health outcomes research at the Glen and the Montreal General Hospital sites of the MUHC. Its research facilities offer a dynamic multidisciplinary environment that fosters collaboration and leverages discovery aimed at improving the health of individual patients across their lifespan. The RI-MUHC is supported in part by the Fonds de recherche du Québec – Santé (FRQS). rimuhc.ca
CSHL Contact:
Dagnia Zeidlickis
516-367-6846
zeidlick@cshl.edu
Feinstein Contact:
Matthew Libassi
516-465-832
mlibassi@northwell.edu
RI-MUHC Contact:
Fabienne Landry
514-812-7722
fabienne.landry@muhc.mcgill.ca