
Fil d'Ariane
- Nouvelles et événements
- Nouvelles
- Content
- Un nouvel essai de thérapie génique suscite l’espoir chez les patients atteints d’une maladie métabolique rare
null Un nouvel essai de thérapie génique suscite l’espoir chez les patients atteints d’une maladie métabolique rare
Dernière mise à jour par Communications le 3 mars 2020
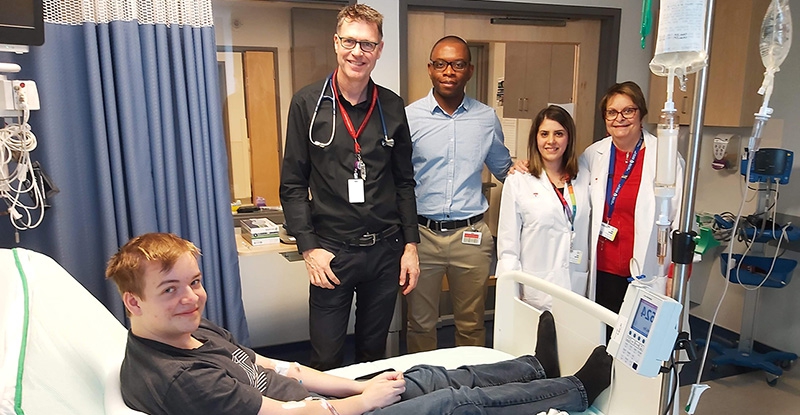
Source : CUSM. À 18 ans seulement, Samuel Gauthier est déjà un pionnier pour les patients qui espèrent de nouvelles options de traitement pour gérer une maladie extrêmement rare. Samuel est le premier patient canadien et le neuvième dans le monde à participer à la seconde phase d’un essai clinique qui utilise la thérapie génique pour traiter la glycogénose de type 1, aussi appelée « GSD 1 ».
Samuel fait partie des quelque 6 000 patients dans le monde, dont 20 au Québec, connus pour vivre avec ce désordre métabolique génétique rare, caractérisé par une incapacité à décomposer le glycogène (une forme de sucre entreposé dans l’organisme) pour fabriquer du glucose. « En fait, mon corps n’est pas capable de produire du glucose ou de l’entreposer comme les autres », explique-t-il. Cette situation l’expose à un risque constant d’hypoglycémie (faible taux de sucre dans le sang), qui peut l’amener à se sentir étourdi, faible et affamé s’il ne mange pas toutes les 2 ou 3 heures. Une situation qui risque aussi de provoquer des convulsions et même la mort si son cerveau venait à manquer de glucose pendant de longues périodes de jeûne.
« Quand nous jeûnons, nous avons besoin de carburant exploitable. Une fois que nous avons utilisé le glucose présent dans notre sang, notre organisme peut utiliser le glycogène, qui est un surplus de glucose gardé en réserve (en banque) pour un usage futur », explique le Dr John Mitchell, directeur de la division d’endocrinologie de l’Hôpital de Montréal pour enfants (HME) et expert des maladies métaboliques rares au Centre universitaire de santé McGill (CUSM). « Dans le cas de Samuel, son organisme ne peut pas garder de glucose en banque. Son corps commence à dégrader le glycogène, mais se met ensuite à produire des sous-produits ou produits chimiques toxiques. En plus de l’hypoglycémie, cela peut entraîner une élévation des lipides, des triglycérides, du lactate et de l’acide urique dans son corps. Ces composés chimiques présents en concentrations élevées peuvent causer la goutte et entraîner des dommages à long terme aussi bien à son foie qu’à ses reins. »
Jusqu’à maintenant, le seul traitement disponible pour les patients comme Samuel comporte deux volets : une surveillance constante des taux de glucose pour s’assurer que sa glycémie est à un niveau optimal, et l’ingestion planifiée de boissons contenant des ingrédients précis pour aider à maximiser le contrôle de la glycémie, la nutrition et l’énergie.
« Samuel s’en remet à des repas fréquents, et ce, depuis l’enfance, explique le Dr Mitchell. Ses boissons sont composées de 30 à 40 grammes d’amidon de maïs cru mélangés à une formule de lait de soya, qu’il prend toutes les 2 ou 3 heures, se levant même la nuit pour en boire. Comme l’amidon de maïs est un glucide complexe, il fournit une quantité constante de glucose qui est digéré plus lentement que les autres options. Administré tout au long de la journée ou de la nuit, il peut aider à maintenir la glycémie à des taux normaux. »
Mais le fait de devoir respecter un horaire d’alimentation rigide pendant toute une vie a des effets importants sur la qualité de vie du patient et de sa famille. « Comme vous pouvez l’imaginer, l’idée que les taux puissent chuter pendant la nuit est extrêmement stressante pour les familles, souligne le Dr Mitchell. Il n’est pas rare que des patients et membres de la famille se disent très inquiets de la gestion et du contrôle de la maladie. Quand on ajoute à cela le manque de sommeil, ça bouleverse vraiment la qualité de vie. »
C’est un sentiment partagé par Samuel, qui a dû se soumettre à un horaire de repas et de sommeil très strict pour gérer sa maladie. « Je dois mettre des alarmes la nuit pour me réveiller et prendre mes boissons. Je ne peux pas manger ce que je veux. Je dois toujours faire attention à mes taux de glucose, et il faut toujours que je traîne un sac à dos rempli de tout ce que j’ai besoin où que j’aille. Ce serait formidable de ne pas avoir à me réveiller toutes les quelques heures et de ne pas toujours penser à une possible baisse. »
Un essai de thérapie génique offre une lueur d’espoir
Quand Samuel a eu 18 ans, il a quitté les soins pédiatriques. Il a alors montré un vif intérêt pour un nouvel essai clinique offert par le service de génétique médicale au CUSM — le seul centre participant à cet essai au Canada — ayant le potentiel de trouver de nouvelles avenues pour gérer une maladie qui, bien que rare, affecte grandement la vie de sa famille et celles de milliers d’autres.
« Dès que le Dr Mitchell m’a parlé de cette option, j’ai été intéressé et j’ai voulu y participer, dit Samuel. C’était ma chance, et je l’ai saisie. »
Le Dr Mitchell a fait part des détails de l’étude à Samuel, expliquant qu’il s’agirait de la première série d’essais sur des humains. « C’est un petit essai, comptant seulement 9 à 12 patients dans le monde, explique-t-il. L’objectif est de voir si l’injection dans l’organisme de plus d’un billion de particules virales contenant l’ADN du gène qui manque à Samuel peut aider son organisme à décomposer le glycogène. Cette phase particulière de l’essai examine l’innocuité et l’efficacité de la dose de particules virales. Mais un second objectif demeure : est-ce que ça fonctionne? »
Le 4 décembre 2019, Samuel a reçu une perfusion unique devant apporter une nouvelle copie du gène manquant jusqu’à son foie par le biais d’un virus naturel. Pour vérifier si le traitement fonctionne, Samuel a accepté de subir des analyses sanguines, des examens d’imagerie médicale, des examens physiques et des ECG sur une base régulière pendant deux à trois mois. Il s’agit d’un protocole de recherche rigoureux qui fournira, au Dr Mitchell et à l’équipe derrière l’étude, des données précieuses pour vérifier si la dose était efficace et voir comment le corps a répondu.
« Tout au long de l’essai, nous allons essayer de diminuer la quantité d’amidon de maïs qu’il prend et attendre que ses taux chutent (apparition d’une hypoglycémie) pour voir combien de temps il peut jeûner avec une dose fixe d’amidon de maïs, précise le Dr Mitchell. Si l’injection donne les résultats que nous espérons, on croit qu’on pourrait augmenter la durée pendant laquelle Samuel peut jeûner à 6, 8 et peut-être même 12 heures – ce qui offrirait un sommeil beaucoup plus réparateur et une plus grande souplesse dans la prise en charge de la maladie. Nous ne savons pas si ça va fonctionner ni combien de temps l’effet pourrait durer – que ce soit un an ou toute sa vie. Mais, si ça fonctionne, ça pourrait améliorer grandement sa qualité de vie. »
« Les choses se passent bien et je me considère chanceux d’avoir eu cette chance », rapporte Samuel, qui continue à participer à des groupes Facebook destinés aux patients qui sont devenus experts dans la prise en charge d’une maladie peu connue. « J’ai hâte de connaître les résultats de l’étude pour voir si le traitement a fonctionné. »
« C’est important de participer à ces études parce que ça donne de l’espoir à nos patients, et une occasion de prendre part à quelque chose qui peut être bénéfique, explique le Dr Mitchell. Nous progressons dans la compréhension de cette maladie, et pour moi c’est quelque chose de vraiment passionnant. »